Acidi Grassi Omega-3

Il termine omega-3 (n-3) è utilizzato per descrivere la struttura di una famiglia di acidi grassi polinsaturi (PUFA). La sigla "n-3" indica la posizione del primo doppio legame che è in posizione 3 contando dal carbonio terminale. Come gli altri acidi grassi, gli omega 3 hanno nomi sistematici e comuni, ma sono spesso indicati con una nomenclatura "scorciatoia o semplificata" che indica il numero di atomi di carbonio nella catena, il numero di doppi legami e la posizione del primo doppio legame rispetto al carbonio terminale. Il più semplice degli acidi grassi n-3 è l'alfa-linolenico (18: 3n-3). L'acido alfa-linolenico è sintetizzato a partire dall'acido n-6 linoleico (18: 2n-6) tramite desaturazione catalizzata dall'enzima delta-15 desaturasi. Gli animali, compresi gli esseri umani, non possiedono questo enzima e quindi non sono in grado di sintetizzare l'acido alfa-linolenico.
Al contrario, le piante possiedono il delta-15 desaturasi e quindi sono in grado di sintetizzarlo. Anche se gli animali non lo possono sintetizzare, lo possono metabolizzare tramite un'ulteriore desaturazione e allungamento. La deidrogenazione avviene in atomi di carbonio al di sotto dell'atomo di carbonio numero 9 (contando dal carbonio carbossilato) e soprattutto si verifica nel fegato. L'acido alfa-linolenico può essere convertito in acido stearidonico (18: 4n-3) dall'enzima delta-6 deidrogenato e successivamente può essere allungata ad acido eicosatetraenoico (20: 4n-3), che può essere ulteriormente deidrogenato dall'enzima delta-5 desaturasi per produrre acido eicosapentaenoico (20: 5n-3, noto come EPA).
È importante notare che la conversione di acido alfa-linolenico in EPA è in concorrenza con la conversione dell'acido linoleico in acido arachidonico (20: 4n-6), poiché sono utilizzati gli stessi enzimi. La reazione della delta-6 desaturasi è limitante in questo percorso; il substrato preferito per la delta-6 desaturasi è l'acido alfa-linolenico. Tuttavia, l'acido linoleico è molto più abbondante nella maggior parte delle diete umane di quanto non sia l'acido alfa-linolenico e, per questo motivo, il metabolismo degli acidi grassi n-6 è quantitativamente il più importante. Le attività di delta-5 e delta-6 desaturasi sono regolate a seconda dello stato nutrizionale, dagli ormoni ed è inibito dai prodotti finali di reazione, tramite un processo di feedback negativo. Il percorso per la conversione di EPA in acido docosaesaenoico (22: 6n-3, noto come DHA) comporta:
a. l'aggiunta di due atomi di carbonio all'EPA con la formazione dell'acido docosapentaenoico (22: 5n-3, noto come DPA);
b. con aggiunta di due ulteriori carboni si ottiene l'acido 24: 5n-3;
c. la desaturazione nella posizione delta-6 forma l'acido 24: 6n-3;
d. in seguito, avviene la traslocazione di 24: 6n-3 dal reticolo endoplasmatico ai perossisomi;
e. nei perossisomi due carboni vengono rimossi, tramite beta-ossidazione (via metabolica di degradazione degli acidi grassi), per produrre DHA.
EPA, DPA e DHA sono presenti in quantità significative nel pesce e, in quantità minori, nelle foglie verdi, in alcuni oli vegetali, noci e semi. In genere, gli effetti osservati suggeriscono che i PUFA n-3 (PolyUnsatured Fatty Acid, ovvero acidi grassi polinsaturi) agiscono in modo anti-infiammatorio e gli studi più recenti suggeriscono il loro coinvolgimento nella risoluzione dell'infiammazione. Questo avviene tramite:
- Diminuzione della chemiotassi (processo mediante il quale i leucociti si muovono verso un sito di attività infiammatoria in risposta al rilascio di sostanze chimiche) dei neutrofili e monociti verso vari chemo-attrattori compreso LTB 4 (derivato dell'acido arachidonico), peptidi batterici e siero umano[1,2,3,4,5,6]. Il meccanismo con cui inibiscono la chemiotassi non è chiaro, ma può riguardare la riduzione dell'espressione o l'antagonismo dei recettori chemio-attrattivi.
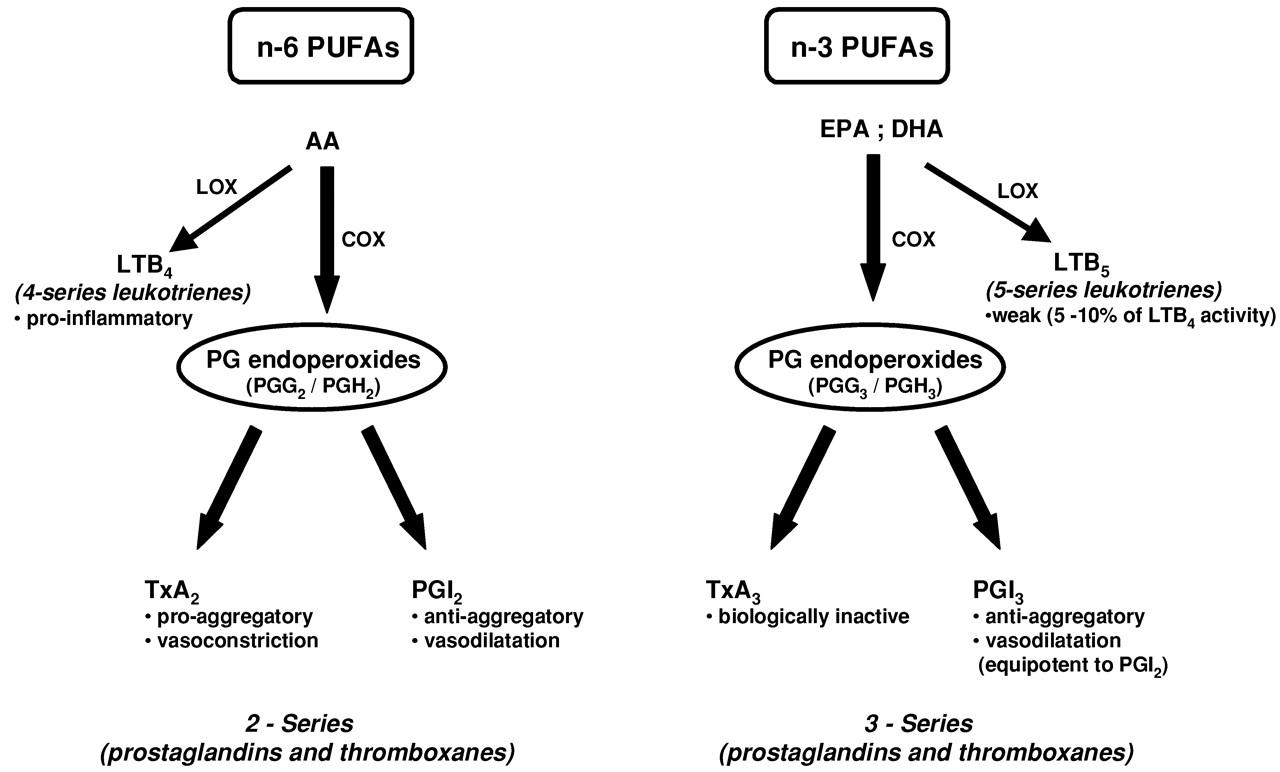
- Diminuzione della produzione di eicosanoidi derivanti dall'acido arachidonico, come le PGE 2 (un tipo di prostaglandina). Diversi studi dimostrano che l'assunzione di omega-3, da una corretta alimentazione, può ridurre la produzione di eicosanoidi che promuovono l'infiammazione[7]. Poiché EPA è un acido grasso altamente insaturo a 20 atomi di carbonio, è anche un substrato per la COX (ciclossigenasi), LOX (lipossigenasi) e citocromo P450 che producono eicosanoidi. Tuttavia, i mediatori prodotti hanno una struttura diversa da quelle a base di acido arachidonico, e si formano prostaglandine (es. PGE 3) e trombossani utili per il nostro organismo che sono coinvolti nell'omeostasi gastrointestinale, renale e piastrinica.
- Inibizione della produzione di endotossine stimolata da IL-6 e IL-8 da parte di cellule endoteliali in coltura umana (da uno studio con utilizzo di EPA e DHA)[8,9], mentre il solo EPA ha inibito la produzione di TNF-alfa indotta da endotossine, da monociti in coltura[10,11]. Un regime alimentare con olio di pesce, in topi da laboratorio, ha favorito la diminuzione della produzione di TNF-alfa, IL-1beta e IL-6 da macrofagi stimolati da endotossine[12,13,14] e diminuito i livelli di TNF-alfa, IL-1beta e IL-6 circolanti in topi iniettati con endotossine.
 Oltre a questo, studi sperimentali e clinici hanno documentato che gli acidi grassi Omega-3 sopprimono la produzione epatica di lipoproteine ricche in trigliceridi e ne accelerano, in parte, la rimozione. L'azione sulla produzione dei trigliceridi avviene in massima parte a livello dell'epatocita ed è legata ad una ridotta produzione di apolipoproteina B, la parte proteica delle VLDL. Ne consegue una ridotta immissione in circolo di trigliceridi. La somministrazione di acidi grassi della serie Omega-3 porta ad una riduzione significativa della trigliceridemia influenzando dunque i livelli di uno dei principali fattori di rischio lipidico per malattie vascolari[15].
Oltre a questo, studi sperimentali e clinici hanno documentato che gli acidi grassi Omega-3 sopprimono la produzione epatica di lipoproteine ricche in trigliceridi e ne accelerano, in parte, la rimozione. L'azione sulla produzione dei trigliceridi avviene in massima parte a livello dell'epatocita ed è legata ad una ridotta produzione di apolipoproteina B, la parte proteica delle VLDL. Ne consegue una ridotta immissione in circolo di trigliceridi. La somministrazione di acidi grassi della serie Omega-3 porta ad una riduzione significativa della trigliceridemia influenzando dunque i livelli di uno dei principali fattori di rischio lipidico per malattie vascolari[15].
In conclusione, EPA e DHA sono i principali PUFA n-3 presenti nel pesce e integratori oleosi derivanti da questi. C'è una sostanziale evidenza che questi acidi grassi sono in grado di inibire parzialmente alcuni aspetti dell'infiammazione, ma vi è la necessità di saperne di più circa le azioni dei PUFA n-3 nei pazienti con malattie infiammatorie, al fine di ottimizzare una strategia per il loro uso terapeutico. In particolare, è necessaria una migliore comprensione della relazione dose-risposta a diversi gruppi di pazienti e di quei fattori che limitano l'efficacia dell'EPA e DHA.
Fonti bibliografiche.
1. Lee TH, Hoover RL, Williams JD, Sperling RI, Ravalese J, 3rd, Spur BW, Robinson DR, Corey EJ, Lewis RA, Austen KF. Effects of dietary enrichment with eicosapentaenoic acid and docosahexaenoic acid on in vitro neutrophil and monocyte leukotriene generation and neutrophil function. N Engl J Med. 1985;312:1217–1224.
2. Endres S, Ghorbani R, Kelley VE, Georgilis K, van der Lonnemann G, Meer JMW, Cannon JG, Rogers TS, Klempner MS, Weber PC, Schaeffer EJ, Wolff SM, Dinarello CA. The effect of dietary supplementation with n?3 polyunsaturated fatty acids on the synthesis of interleukin?1 and tumor necrosis factor by mononuclear cells. N Engl J Med. 1989;320:265–271.
3. Sperling RI, Benincaso AI, Knoell CT, Larkin JK, Austen KF, Robinson DR. Dietary ??3 polyunsaturated fatty acids inhibit phosphoinositide formation and chemotaxis in neutrophils. J Clin Invest. 1993;91:651–660.
4. Schmidt EB, Pedersen JO, Ekelund S, Grunnet N, Jersild C, Dyerberg J. Cod liver oil inhibits neutrophil and monocyte chemotaxis in healthy males. Atherosclerosis. 1989;77:53–57.
5. Schmidt EB, Varming K, Pedersen JO, Lervang HH, Grunnet N, Jersild C, Dyerberg J. Long term supplementation with n?3 fatty acids, ii: effect on neutrophil and monocyte chemotaxis. Scand J Clin Lab Invest. 1992;52:229–236.
6. Luostarinen R, Siegbahn A, Saldeen T. Effect of dietary fish oil supplemented with different doses of vitamin E on neutrophil chemotaxis in healthy volunteers. Nutr Res. 1992;12:1419–1430.
7. Chapkin RS, Akoh CC, Miller CC. Influence of dietary n?3 fatty acids on macrophage glycerophospholipid molecular species and peptidoleukotriene synthesis. J Lipid Res. 1991;32:1205–1213.
8. De Caterina R, Cybulsky MI, Clinton SK, Gimbrone MA, Libby P. The omega?3 fatty acid docosahexaenoate reduces cytokine?induced expression of proatherogenic and proinflammatory proteins in human endothelial cells. Arterioscler Thromb. 1994;14:1829–1836.
9. Khalfoun B, Thibault F, Watier H, Bardos P, Lebranchu Y. Docosahexaenoic and eicosapentaenoic acids inhibit in vitro human endothelial cell production of interleukin?6. Adv Exp Biol Med. 1997;400:589–597.
10. Lo CJ, Chiu KC, Fu M, Lo R, Helton S. Fish oil decreases macrophage tumor necrosis factor gene transcription by altering the NF kappa B activity. J Surg Res. 1999;82:216–221.
11. Zhao Y, Joshi?Barve S, Barve S, Chen LH. Eicosapentaenoic acid prevents LPS?induced TNF?alpha expression by preventing NF?kappaB activation. J Am Coll Nutr. 2004;23:71–78.
12. Yaqoob P, Calder PC. Effects of dietary lipid manipulation upon inflammatory mediator production by murine macrophages. Cell Immunol. 1995;163:120–128.
13. Billiar T, Bankey P, Svingen B, Curran RD, West MA, Holman RT, Simmons RL, Cerra FB. Fatty acid uptake and Kupffer Cell function: fish oil alters eicosanoid and monokine production to endotoxin stimulation. Surgery. 1988;104:343–349.
14. Renier G, de Skamene E, Sanctis J, Radzioch D. Dietary n?3 polyunsaturated fatty acids prevent the development of atherosclerotic lesions in mice: modulation of macrophage secretory activities. Arterioscler Thomb. 1993;13:1515–1524.
15. ALESSANDRO FILIPPI Medico Generale, Responsabile Nazionale Area Cardiovascolare, Società Italiana di Medicina Generale. PUFA e Trigliceridi.