I ROS per combattere il cancro?
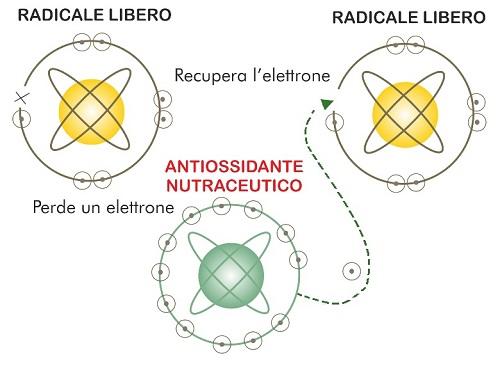
Nella prevenzione e nella lotta contro il cancro si sono sempre indicati come alleati fondamentali gli agenti antiossidanti presenti in integratori e negli alimenti. Addirittura, molti alimenti sono considerati veri e propri “superfood” o “nutraceutici” proprio per la loro concentrazione elevata di sostanze che combattono l’azione dei radicali liberi. I ROS sono le specie reattive dell’ossigeno e sono un sottogruppo di radicali liberi che si formano normalmente nel nostro organismo in seguito a processi fisiologici quali la fosforilazione ossidativa, la difesa immunitaria e reazioni enzimatiche. La biologia del tumore ha rivelato che le cellule tumorali sono note per esibire un elevato stress ossidativo intrinseco. Rispetto alle cellule sane, la maggior parte di quelle neoplastiche hanno una quantità di specie reattive dell'ossigeno molto più elevata, quali anione superossido, H2O2 e radicali idrossilici[1-4].
Queste sostanze chimiche reattive contenenti ossigeno reagiscono con acidi nucleici, proteine e lipidi, contribuendo in maniera determinante alla proliferazione delle cellule tumorali, alle alterazioni del DNA, all’apoptosi, la metastatizzazione, l’angiogenesi e l’alternanza nella sensibilità cellulare per agenti antitumorali[5,6].
La disfunzione dei telomeri, osservata nelle cellule tumorali, è associata ad alterata biogenesi e funzionalità mitocondriale che porta all’aumento della produzione di ROS[7]. Coerentemente con questa relazione, vale la pena notare che l’aumento dei ROS è legato all’invecchiamento[8]. Il processo di invecchiamento è caratterizzato da una diminuzione della componente antiossidante dell’organismo e questo permette ai radicali liberi di agire negativamente sulla funzionalità del nostro corpo.
Una notizia pubblicata sulla rivista Open Biology non è dello stesso parere e mette sotto accusa il ruolo degli antiossidanti nel combattere il cancro e il processo di invecchiamento. Il premio Nobel James Watson, padre della scoperta del Dna con Francis Crick, sostiene che assumere anti-ossidanti durante le comuni terapie antitumorali potrebbe annullare l’effetto delle cure. Questa tesi si basa sul fatto che alcuni trattamenti chemioterapici antineoplastici e la radioterapia producono radicali liberi e specie estremamente reattive per arrecare danni alla cellula tumorale e favorirne la morte. Secondo il dott. Watson, integrare con antiossidanti significa annullare il meccanismo d’azione della terapia antitumorale.
Questa teoria sembra più una provocazione che un qualcosa di veritiero e utile per combattere la progressione del cancro. Prevenire l’invecchiamento e i danni al DNA è fondamentale per contrastare la carcinogenesi. Su questo sito abbiamo già pubblicato un articolo sull’utilità di digiunare nel periodo pre- e post-chemioterapia (Digiuno prima e dopo la chemioterapia) proprio a questo scopo. Arrivare però a dire che i ROS potrebbero essere un qualcosa di utile nella lotta contro il cancro è come dire che il tabagismo può essere un sistema di prevenzione del tumore del polmone!
Fonti bibliografiche
1. Kawanishi S, Hiraku Y, Pinlaor S, Ma N. Oxidative and nitrative damage in animals and patients with inflammatory diseases in relation to inflammation-related carcinogenesis. Biol Chem. 2006;387(4):365–372.
2. Szatrowski TP, Nathan CF. Production of large amounts of hydrogen peroxide by human tumor cells. Cancer Res. 1991;51:794–798. Evidence of the increased level of H2O2 in human cancer cells.
3. Hileman EO, Liu J, Albitar M, Keating MJ, Huang P. Intrinsic oxidative stress in cancer cells: a biochemical basis for therapeutic selectivity. Cancer Chemother Pharmacol. 2004;53:209–219. Publication of amplifying reactive oxygen species (ROS) to increase therapeutic selectivity.
4. Toyokuni S, Okamoto K, Yodoi J, Hiai H. Persistant oxidative stress in cancer. FEBS Lett. 1995;358:1–3.
5. Arnold RS, Shi J, Murad E, et al. Hydrogen peroxide mediates the cell growth and transformation caused by the mitogenic oxidase Nox1. Proc Natl Acad Sci USA. 2001;98:5550–5555.
6. Ishikawa K, Takenaga K, Akimoto M, et al. ROS-generating mitochondrial DNA mutations can regulate tumor cell metastasis. Science. 2008;320:661–664.
7. Sahin E, Colla S, Liesa M, et al. Telomere dysfunction induces metabolic and mitochondrial compromise. Nature. 2011;470:359–65.
8. Afanas’ev I. Reactive oxygen species signaling in cancer: comparison with aging. Aging Dis. 2011;2:219–230.